
Par Ian Angus
La première partie de cette contribution (voir sur ce site «Crise de l’azote: une menace négligée pour les systèmes assurant la vie de la Terre») explique comment l’activité métabolique des bactéries spécialisées dans le sol et les océans détermine le cycle de l’azote, en «fixant» l’azote inerte de l’air en azote réactif, en le transformant sous des formes que les plantes peuvent utiliser et en le rejetant éventuellement dans l’atmosphère. Cette contribution participe d’une clarification sur un aspect important, parmi d’autres, de la faille métabolique, autrement dit de la rupture entre «les activités humaines» et «la nature» qui s’est accélérée dès la seconde moitié du XXe siècle.
Comme l’expliquent les scientifiques de l’Institut Max Planck en Allemagne, le «réseau de recyclage de l’azote microbien» a maintenu un niveau constant d’azote réactif dans la biosphère mondiale pendant des milliards d’années.
«Il existe une étonnante diversité de micro-organismes qui transforment l’azote, et chacun de ces micro-organismes a des exigences physiologiques distinctes pour une croissance optimale. Comme les conditions de croissance dans la nature sont très variables et rarement optimales, le renouvellement de l’azote par des micro-organismes individuels est forcément inefficace. Cependant, les transformations de l’azote dans l’environnement sont effectuées par des communautés microbiennes qui recyclent l’azote plus efficacement que les micro-organismes individuels. Par conséquent, très peu d’azote biodisponible s’échappe dans l’atmosphère, et la petite quantité perdue sous forme de diazote gazeux est compensée par la fixation de l’azote.» [1]
Ce cycle vital a été perturbé dans l’Europe du XIXe siècle, lorsque les villes sont devenues si grandes que l’azote et les autres nutriments consommés dans les aliments par la population urbaine ne pouvaient plus retourner dans la terre, ce qui a provoqué la pollution dans les villes et réduit la fertilité des sols dans les campagnes. Ce que Marx appelait «une faille irréparable dans le processus interdépendant du métabolisme social» [3] a été atténué – dissimulé, mais pas cicatrisé – par l’importation de guano et de nitrates minéraux riches en azote d’Amérique du Sud pour fertiliser les champs, et par la construction de canalisations d’évacuation des déchets urbains pour les diriger vers les rivières et océans.
Cependant, au XXe siècle, les combustibles fossiles et l’agriculture industrielle ont ouvert une brèche encore plus grande en déployant des procédés qui libèrent annuellement dans l’environnement plus de deux fois plus d’azote réactif que ce que la nature seule a jamais produit. En particulier, près de 200 millions de tonnes métriques d’engrais synthétiques sont utilisées chaque année – et la plupart de l’azote réactif qu’ils contiennent s’échappe dans l’environnement, polluant l’air et l’eau et perturbant les écosystèmes.
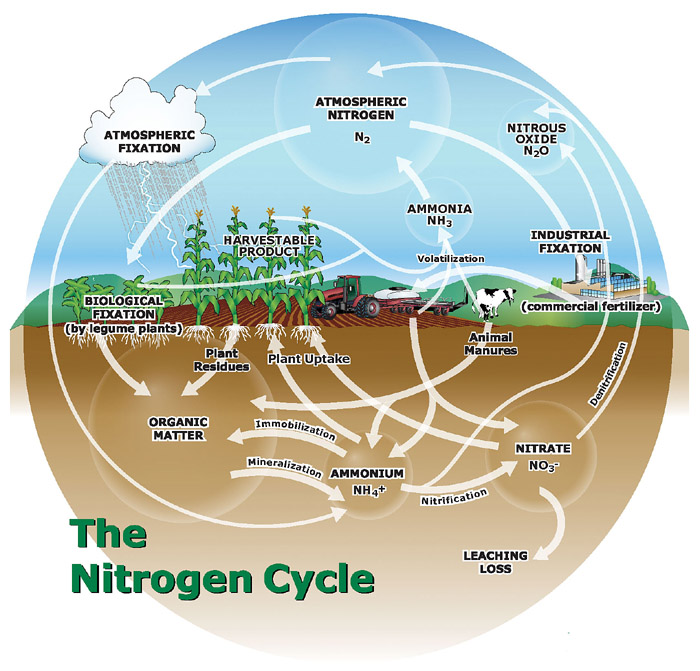
Le schéma publié dans la première partie de cette contribution illustrait comment dans les écosystèmes naturels l’activité bactérienne contrôle l’azote dans le sol. L’introduction des engrais synthétiques, de l’agriculture industrielle et des combustibles fossiles signifie que peu d’écosystèmes de ce type existent encore. La fixation bactérienne naturelle n’est plus la principale source d’azote réactif, et les petites quantités qui ont toujours échappé aux écosystèmes locaux sont devenues un flot qui affecte toute la biosphère. Le graphique ci-dessous, bien qu’encore très simplifié, donne une image plus précise du cycle mondial de l’azote au XXIe siècle:
Les négationnistes du changement climatique affirment souvent que le dioxyde de carbone ne peut pas être nocif parce que les plantes en ont besoin pour pousser. Le même faux argument peut être avancé au sujet de l’azote, et notre réponse est la même: trop d’une bonne chose peut être mortel. Des organismes et des écosystèmes qui ont évolué dans un monde où l’approvisionnement en azote réactif était strictement limité sont aujourd’hui perturbés, dans de nombreux cas détruits, par une surabondance d’azote sans précédent.
Cascades de l’azote
L’accumulation croissante de dioxyde de carbone dans l’atmosphère peut être mesurée directement – elle a récemment dépassé 413 parties par million, une concentration nettement plus élevée qu’à tout autre moment au cours des 800’000 dernières années. Déterminer la relation exacte entre les niveaux de CO2 et les températures globales est un processus complexe, mais il ne fait aucun doute que plus de CO2 équivaut à des températures plus élevées.
Il n’existe aucun moyen équivalent de suivre l’accumulation de l’azote réactif ou de résumer ses effets environnementaux en termes simples. Contrairement au dioxyde de carbone, la plupart des produits chimiques formés par l’azote réactif peuvent facilement se transformer l’un en l’autre, et ils ont des effets différents, selon les conditions locales.
«De nombreux seuils pour la santé humaine et la santé des écosystèmes ont été dépassés en raison de la pollution par l’azote, y compris pour l’eau potable (nitrates), la qualité de l’air (smog, particules, ozone troposphérique), l’eutrophisation des eaux douces, la perte de biodiversité, la diminution de l’ozone stratosphérique, les changements climatiques et les écosystèmes côtiers (zones mortes). Chacun de ces effets environnementaux peut être amplifié par la «cascade de l’azote»: un seul atome d’azote peut déclencher une cascade d’impacts environnementaux négatifs en séquence.» [4]
Toute cascade d’azote donnée peut entraîner une séquence différente de transformations et d’effets chimiques. Par exemple, un atome d’azote qui s’infiltre dans les eaux souterraines à partir d’un sol agricole suivra une trajectoire différente de celle d’un atome d’azote produit par une automobile qui brûle de l’essence, et chacun peut perturber plusieurs processus biogéochimiques. Scientific American illustre ainsi une cascade possible:
- «L’azote produit lors de la combustion des combustibles fossiles peut causer une grave pollution de l’air…
- avant qu’il ne se combine avec l’eau pour créer de l’acide nitrique dans la pluie…
- et s’ajoute à l’azote qui s’échappe des champs fertilisés, des excréments d’animaux d’élevage, des eaux usées humaines et des légumineuses.
- Lorsqu’une trop grande quantité d’azote pénètre dans les écosystèmes terrestres, il peut contribuer au déclin de la biodiversité et peut-être à un risque accru de plusieurs maladies humaines.
- Un seul atome d’azote provenant d’une usine, d’un véhicule ou d’une ferme peut acidifier le sol et contaminer l’eau potable avant de pénétrer dans les rivières…
- où il peut se rendre dans les océans et contribuer à alimenter les proliférations d’algues toxiques et les zones côtières mortes.
- A n’importe quel point de cette chaîne, les bactéries peuvent transformer l’atome solitaire en oxyde nitreux, un puissant gaz à effet de serre qui accélère également la perte de l’ozone stratosphérique protecteur. Seules les bactéries qui reconvertissent l’atome en gaz N2 inoffensif peuvent en arrêter les effets néfastes.» [5]
Les cascades d’azote ne sont pas linéaires – les atomes peuvent passer d’une séquence à l’autre, en tout ou en partie, ou répéter une étape, ou passer à une autre séquence, sur des périodes allant de quelques secondes à plusieurs décennies. Mais l’effet global peut se résumer ainsi : plus l’azote réactif dans l’environnement entraîne plus de cascades d’azote et plus de perturbations de la biosphère.
Le graphique ci-dessous du Scientific American illustre les 5 premières séquences («La face sombre de l’azote»)
WAGES de l’azote
Comme le soulignent les auteurs du rapport European Nitrogen Assessment (Rapport européen d’évaluation de l’azote) en 2011, «il existe une grande diversité de formes de polluants azotés… entraînant de nombreux polluants secondaires (dont de nombreuses formes d’azote organique dans l’eau et l’air) et une liste encore plus longue des effets environnementaux. Le problème de l’azote dans l’environnement présente un degré de complexité que peu de scientifiques sont en mesure de couvrir entièrement» [6]. Ils ont résumé les menaces environnementales posées par l’azote réactif excessif en utilisant l’acronyme WAGES – Water, Air, Greenhouse balance, Ecosystems, Soil / eau, air, bilan d’émission de gaz à effet de serre, écosystème, sols – et ont consacré un chapitre à chacun de ces éléments.
Le rapport de 2013 intitulé Our Nutrient World (Notre monde nutritif) donne un aperçu des menaces qui pèsent sur WAGES, y compris les effets de l’azote (N) et du phosphore (P).
«Qualité de l’eau. Le rejet d’une trop grande quantité d’azote et de phosphore dans l’environnement affecte les écosystèmes marins et d’eau douce par eutrophisation, entraînant des proliférations d’algues, des zones mortes et des mortalités de poissons, tout en polluant les aquifères et en provoquant une eau potable impure. De vastes régions de la plupart des continents sont touchées, alors qu’on estime qu’environ 80% des grands écosystèmes marins sont soumis à une eutrophisation importante dans les eaux côtières. Dans les écosystèmes d’eau douce, on considère généralement que des concentrations de 1 à 2 mg de Nr par litre et de 0,1 mg de P par litre ou moins causent une eutrophisation, mais les concentrations spécifiques dépendent des conditions hydrologiques et climatiques locales.
«Qualité de l’air. L’azote réactif contribue à plusieurs menaces de pollution atmosphérique pour la santé humaine par les émissions d’oxydes d’azote (NOx) et d’ammoniac (NH3), qui entraînent des concentrations élevées de dioxyde d’azote (NO2), de particules (PM) et d’ozone troposphérique (O3) au sol. On estime que 60% de la population mondiale des zones urbaines est exposée aux particules, au NO2 et à d’autres substances toxiques à des niveaux supérieurs aux seuils d’effets nocifs, tandis que 60% de l’augmentation de l’O3 troposphérique depuis 1900 est due aux émissions de NOx, l’O3 troposphérique entraînant également une perte de productivité agricole d’environ 5%.
«Bilan d’émission des gaz à effet de serre. La perturbation des cycles des éléments nutritifs a à la fois des effets de réchauffement et de refroidissement du climat. L’oxyde nitreux (N2O), un gaz à effet de serre, est la composante la plus durable du réchauffement, tandis que le NOx contribue à l’O3 troposphérique, qui entraîne un réchauffement supplémentaire en réduisant l’absorption de CO2 par les plantes. En revanche, les dépôts atmosphériques d’azote favorisent la croissance des plantes et l’absorption de CO2, tandis que l’azote contribue aux particules solubles dans l’eau (PM), qui ont toutes deux des effets de refroidissement. Grâce à des politiques efficaces de réduction des chlorofluorocarbures et d’autres substances appauvrissant la couche d’ozone, le N2O est maintenant la principale cause de l’appauvrissement en O3 stratosphérique, ce qui augmente le risque de cancer de la peau.
«Ecosystèmes et biodiversité. Les menaces d’une trop grande quantité de nutriments impliquent la perte d’espèces à haute valeur pour la conservation et la nourriture qui sont naturellement adaptées à peu de nutriments et qui sont menacées par l’eutrophisation. Les dépôts atmosphériques d’azote dépassent 5 kg par hectare et par an dans la moitié des aires protégées de la CDB [Convention sur la diversité biologique] dans les «points chauds de la biodiversité mondiale» et les écorégions du G200 [soit les 238 régions écologiques définies par le World Wildlife Fund], et on estime qu’ils représentent de 5 à 15% de la perte actuelle de biodiversité mondiale. En revanche, les pénuries d’azote et de phosphore dans les agroécosystèmes limitent la productivité et peuvent forcer les agriculteurs à chercher des terres agricoles supplémentaires, ce qui entraîne un empiétement agricole menaçant les écosystèmes vierges.
«Qualité du sol. Un apport excessif d’azote peut conduire à l’acidification des sols, tant dans les écosystèmes semi-naturels et forestiers soumis à des niveaux élevés de dépôts atmosphériques d’azote que dans les écosystèmes agricoles à taux de fertilisation élevés. Bien que cela puisse être atténué par l’ajout de chaux dans les agroécosystèmes, l’effet tend à appauvrir les éléments essentiels du sol dans les sols naturels, tout en mobilisant les métaux toxiques, ce qui entraîne des risques supplémentaires pour la santé des forêts et les populations de poissons d’eau douce. Une disponibilité insuffisante des éléments nutritifs dans l’agriculture entraîne une perte de fertilité des sols et peut exacerber l’érosion, tandis que les pénuries de micronutriments peuvent également limiter l’utilisation efficace des ressources disponibles en azote et en phosphore.» [7]
Comme le montre cette énumération, il y a peu de problèmes écologiques (s’il y en a) qui n’ont pas de composante azotée, qui n’ont pas été initiés ou aggravés par l’expansion massive de l’azote réactif dans le sol, l’air et l’eau. Des études récentes montrent que ses effets néfastes seront intensifiés par le changement climatique [8].
[…] Le point essentiel est que la surabondance d’azote (et la répartition inégale qui provoque des pénuries dans certaines régions, en particulier en Afrique subsaharienne) endommage la biosphère de nombreuses façons. Il est douloureusement clair que tout effort sérieux visant à prévenir les catastrophes écologiques au cours de ce siècle doit inclure la réduction de la surproduction d’azote réactif.
Pour déterminer comment cela peut être fait, nous devons comprendre comment et pourquoi la surabondance s’est produite. Comment la faille métabolique dans l’agriculture du XIXe siècle, caractérisée par l’épuisement et le gaspillage des nutriments essentiels, a-t-elle conduit au XXe siècle à des failles planétaires causées par une surabondance et une utilisation excessive des mêmes éléments? Dans un troisième article sera abordée cette question. (Article publié par Ian Angus dans une série disponible sur son site Climate & Capitalism; traduction rédaction A l’Encontre)
Notes
[1] Marcel M. M. Kuypers, Hannah K. Marchant, and Boran Kartal, “The Microbial Nitrogen-cycling Network,” Nature Reviews: Microbiology 16, no. 5 (2018): 271.
[2] Ian Angus, “Cesspools, Sewage, and Social Murder: Environmental Crisis and Metabolic Rift in Nineteenth Century London,” Monthly Review, July-August 2018: 32-68.
[3] Karl Marx, Capital, vol. 3 (London: Penguin, 1981): 949-50.
[4] J.W. Erisman et al., “Consequences of Human Modification of the Global Nitrogen Cycle,” Philosophical Transactions of the Royal Society B: Biological Sciences 368, no. 1621 (July 2013)
[5] Alan R. Townsend and Robert W. Howarth, “Fixing the Global Nitrogen Problem,” Scientific American 302, no. 2 (February 2010); 65-6.
[6] Mark A. Sutton et al., “The Challenge to Integrate Nitrogen Science and Policies,” The European Nitrogen Assessment: 84.
[7] Mark A. Sutton et al., Our Nutrient World: The Challenge to Produce More Food and Energy with Less Pollution. (Edinburgh: Centre for Ecology and Hydrology, 2013), 32-3. “G200 ecoregions” are locations identified by the conservation group WWF as priorities.
[8] Richard Conniff, “The Nitrogen Problem: Why Global Warming Is Making It Worse,” Yale Environment 360, August 7, 2017.



Soyez le premier à commenter