Par Ian Angus
«La désoxygénation des océans est le troisième membre, mais moins signalé, d’une trinité diabolique du changement climatique, avec le réchauffement climatique et l’acidification des océans. Il ne s’agit pas tant d’une autre chaussure qui se détache de nos émissions de CO2 que d’une grosse botte qui donne un coup de pied dans les écosystèmes océaniques, avec des répercussions importantes sur des centaines de millions de personnes qui dépendent des océans pour vivre, et avec des rétroactions sur le climat.» – Skeptical Science [1]
Deuxième partie: manque d’oxygène
Poursuite de l’examen par Ian Angus du «trio mortel» des attaques au CO2 contre la vie océanique. [Voir la première partie sur ce site.]
L’océan perd son souffle, ce qui a des effets mortels sur la vie marine et les cycles biogéochimiques qui façonnent l’ensemble de la biosphère.
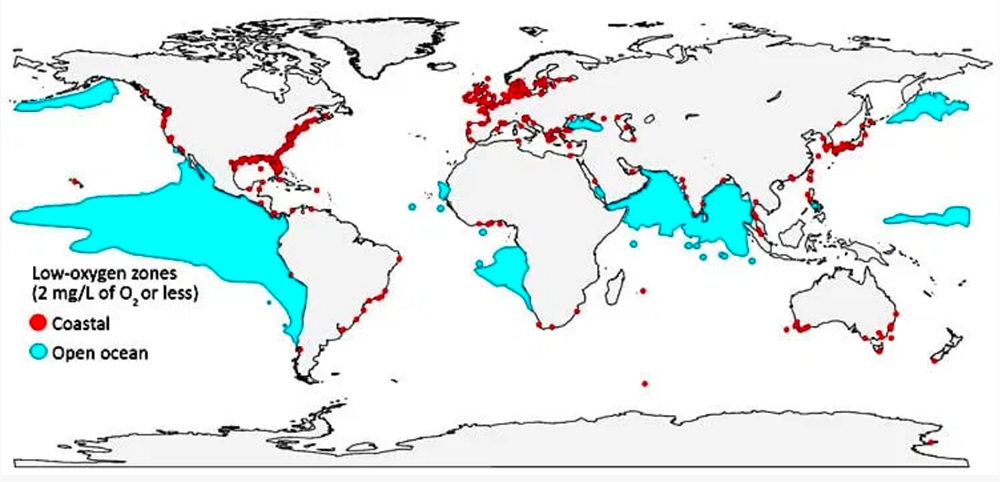
Depuis 1960, les zones à faible teneur en oxygène en haute mer ont augmenté de 4,5 millions de kilomètres carrés, soit une superficie de la taille de l’Union européenne. Certaines régions ont perdu 40% de leur oxygène, et le volume d’eau ne contenant pas d’oxygène a plus que quadruplé. L’océan perd environ un milliard de tonnes d’oxygène chaque année. Au rythme actuel, le déclin de l’oxygène océanique, source de vie, va tripler d’ici à 2100. Si l’on ajoute à cela le nombre croissant de zones côtières mortes, on obtient une situation d’urgence en matière de maintien de la vie.
Dans l’ensemble, la teneur en oxygène de l’océan n’a diminué que de 2%, mais ce déclin s’est produit presque entièrement dans les parties de l’océan où la vie marine est généralement la plus abondante, de sorte que son impact est bien plus important que ce pourcentage ne le laisse supposer.
Les articles précédents de cette série étendue sur les failles métaboliques ont examiné deux gouffres écologiques créés par la poussée inhérente au capitalisme de se développer à tout prix: la surabondance d’azote créée par la dépendance de l’agriculture industrielle aux engrais chimiques de synthèse, et la surabondance de dioxyde de carbone créée par la dépendance du capitalisme aux combustibles fossiles [voir sur ce site les articles ayant trait à ces deux thèmes publiés en date du 21 août 2020 et du 21 février 2020]. Toutes deux perturbent les cycles biogéochimiques qui ont façonné la biosphère pendant des centaines de millions d’années, provoquant des failles sans précédent dans le métabolisme du système terrestre.
La crise de l’oxygène des océans est due aux résidus d’azote et de dioxyde de carbone présents dans différentes parties de l’océan.
Dans les zones côtières et les estuaires, des millions de tonnes d’engrais azotés synthétiques transportés par les rivières créent des zones mortes saisonnières dans les zones côtières du monde entier. Environ 900 de ces zones ont été identifiées, et il y en a sans doute des centaines d’autres. Les scientifiques étudient les zones mortes côtières depuis les années 1980 et il existe un large consensus sur leurs causes et leurs effets.
Cet article se concentre sur une évolution parallèle qui n’a été étudiée que depuis une quinzaine d’années: la croissance des zones hypoxiques (à faible teneur en oxygène) et anoxiques (à teneur nulle en oxygène) en haute mer, causée par le réchauffement climatique. Elles ne sont pas toujours physiquement séparées des zones mortes côtières – dans la mer Baltique et la mer d’Arabie [ou mer d’Oman], par exemple, elles se chevauchent – mais elles se développent et s’étendent différemment.
***
Tout l’oxygène dissous dans l’eau de mer, quelle que soit sa profondeur, provient de la surface ou de la couche proche de la surface, selon l’un des deux processus suivants.
- Il y a un échange constant de molécules d’oxygène (O2) entre l’atmosphère et l’océan, à l’interface air-mer. En termes simples, l’O2 de l’air se dissout dans l’eau et l’O2 de l’eau fait des bulles dans l’air.
- Les plantes, en particulier le phytoplancton, qui poussent sur et dans l’eau, produisent beaucoup plus d’O2. La photosynthèse nécessite la lumière du soleil, et même dans une eau très claire, la lumière pénètre à moins de 200 mètres de profondeur. Cette zone euphotique (euphotic est le mot grec pour «bien éclairé») est à l’origine de près de la moitié de l’oxygène mondial et de la majeure partie de l’approvisionnement des océans.
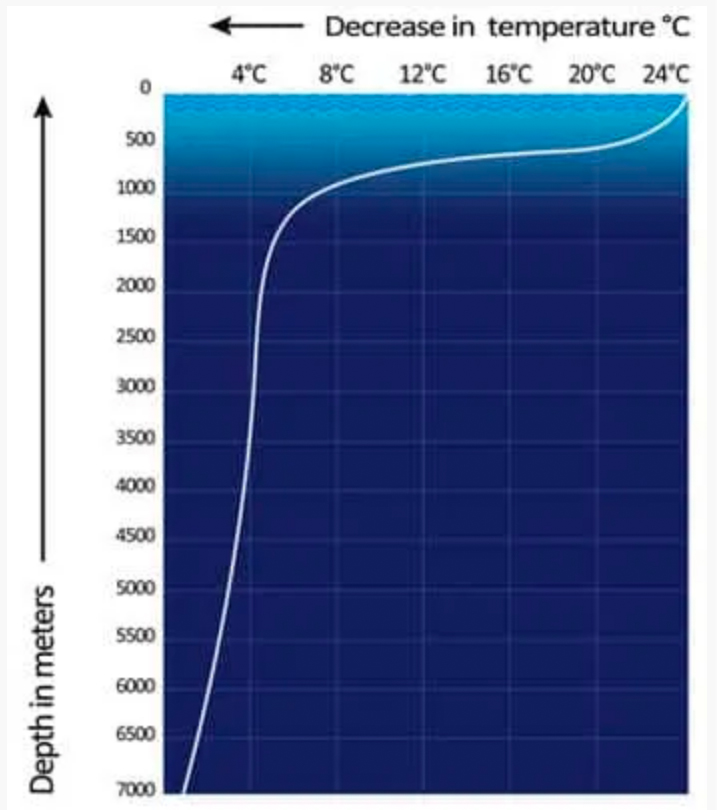
Dans la majeure partie de l’océan, les 200 mètres supérieurs environ sont appelés la couche de surface ou couche mixte. Les vagues, les courants dus au vent et la convection agitent constamment son contenu, ce qui rend sa température, sa salinité et sa teneur en gaz dissous à peu près uniformes. L’oxygène dissous se répand à travers la couche mélangée relativement rapidement et uniformément.
La couche mélangée est chauffée directement par la lumière du soleil et est constamment alimentée par l’eau douce des rivières, la pluie et la fonte des glaces. Elle est donc plus légère (moins dense) que l’eau qui se trouve en dessous, où une chute soudaine de température définit la thermocline [zone de transition thermique], soit une couche plus froide et plus dense qui sépare la couche mélangée de la couche profonde froide et très lente qui représente environ 90% du volume et de la masse de l’océan. L’épaisseur de la thermocline varie selon les saisons et la latitude – dans les mers polaires, elle existe à peine avec la couche mélangée – mais dans la plus grande partie de l’océan, elle s’étend de 200 à 1000 mètres sous la surface.
Divers processus connus sous le nom de ventilation déplacent une partie de l’eau mélangée et de l’oxygène qu’elle contient dans la thermocline. La distribution de l’oxygène dépend des courants locaux, régionaux et mondiaux, des marées, de la topographie locale, des turbulences imprévisibles et d’autres facteurs, de sorte qu’elle est inégale. Plus particulièrement, dans certaines parties de la thermocline, la combinaison d’une faible ventilation et de micro-organismes consommateurs d’oxygène donne lieu à des poches appelées zones de minimum d’oxygène (ZMO). À cette profondeur, la plupart des thermoclines regorgent de poissons, mais la vie dans une ZMO est largement limitée aux microbes qui peuvent survivre avec très peu ou pas d’O2.

Un processus différent et beaucoup plus lent joue un rôle majeur dans la distribution de l’oxygène dans les profondeurs de l’océan. Lorsque l’eau gèle dans l’Atlantique Nord, elle laisse du sel derrière elle, créant ainsi une couche de saumure dense qui coule au fond et se déplace lentement vers le sud, apportant tout l’oxygène qu’elle a absorbé à la surface. C’est ainsi que commence le Global Conveyor Belt [circulation thermohaline], un lent courant des grands fonds qui transporte près de 20 millions de mètres cubes d’eau par seconde – 100 fois plus que le fleuve Amazone – en distribuant l’oxygène et les nutriments dans les profondeurs de l’océan. Un circuit complet prend environ 1000 ans. Lorsque l’eau du Groenland atteint le Pacifique Nord, la majeure partie de l’oxygène a disparu: cela contribue à la formation d’une zone de haute mer dans la mer de Béring occidentale et le golfe de l’Alaska.
Le changement climatique contre l’oxygène
Comme nous l’avons vu dans la première partie de cette contribution, l’acidification des océans est le résultat direct de la montée en flèche des émissions de CO2. La désoxygénation des océans a la même cause: les gaz à effet de serre réchauffent le monde, et plus de 90% de cette chaleur supplémentaire a été absorbée par la couche superficielle de l’océan, ce qui réduit l’oxygène total de l’océan et étend les zones minimales d’oxygène.
Des recherches sur les détails de la désoxygénation sont en cours, mais il est clair que le changement climatique est responsable de la majeure partie de l’appauvrissement de l’oxygène en haute mer. Trois processus dépendant de la température – solubilité, stratification et circulation, et métabolismes aérobies – volent la respiration de l’océan.
La solubilité. Lorsque l’eau se réchauffe, elle peut contenir moins d’oxygène dissous. Un volume d’eau donné dans l’Arctique peut absorber plus d’oxygène que le même volume à l’équateur. Si la température de l’eau passe de 4 à 6 °C, la quantité d’oxygène qu’elle peut contenir diminue de 5%.
Pendant de nombreux millénaires, le transfert de gaz dans les deux sens à travers l’interface air-mer était équilibré, de sorte que la quantité d’oxygène dissous dans l’océan est restée à peu près constante. À un moment donné au cours du dernier demi-siècle, cet équilibre a été rompu: l’océan en réchauffement a commencé à libérer plus d’oxygène qu’il n’en absorbait. Une étude récente estime qu’entre 1975 et 2005, la perte nette d’oxygène de l’océan vers l’atmosphère s’est élevée en moyenne à plus d’un milliard de tonnes par an. Si le réchauffement se poursuit, ce dégazage pourrait presque tripler d’ici à 2100 [4].
Stratification et circulation. Comme nous l’avons vu, l’océan est divisé par la température et la salinité en trois couches bien définies, la couche la moins dense se trouvant au-dessus. Le changement climatique a encore réduit la densité de la couche supérieure, en réchauffant l’eau, en augmentant les précipitations et en faisant fondre les glaciers. Il est donc encore plus difficile pour les eaux riches en oxygène de se déplacer vers la thermocline.
Une solubilité réduite signifie qu’il y a moins d’oxygène au total, et une stratification accrue réduit la part de l’oxygène qui circule sous la couche mixte. Depuis 1960, les zones minimales d’oxygène dans la thermocline ont augmenté de 20%, passant d’un peu plus de 25 millions de kilomètres carrés à 30,4 millions – soit 8% de la surface totale de l’océan et 7% de son volume [5].
Le réchauffement climatique affaiblit également la Great Conveyor Belt: la partie nord de l’Atlantique transporte aujourd’hui 15% d’eau en moins qu’en 1960. Jusqu’à présent, aucun effet n’a été mesuré sur les niveaux d’oxygène des océans profonds; cela pourrait refléter la faible vitesse du courant, ou un échantillonnage limité des eaux profondes. On a estimé qu’au rythme actuel de réchauffement, la circulation en eaux profondes diminuera de 45% d’ici à 2100 [6].
Les taux métaboliques. Lorsque la température augmente, presque tous les processus chimiques s’accélèrent, y compris les réactions biochimiques complexes qui maintiennent la vie dans tous les organismes. Les taux métaboliques augmentent proportionnellement à la température – les organismes ont besoin de plus d’oxygène pour maintenir le même niveau d’activité. L’effet est à peine perceptible chez les animaux à sang chaud comme nous, car notre corps utilise toujours une grande quantité d’énergie pour maintenir un état stable. Mais le rythme respiratoire des organismes à sang froid, qui comprennent presque toute la vie marine, augmente considérablement lorsque l’eau se réchauffe [7].
Ainsi, alors qu’une solubilité plus faible et une stratification plus forte réduisent l’apport d’oxygène dissous dans l’eau de mer, la respiration aérobie en augmente la consommation.
Il est difficile de quantifier les impacts relatifs de chacun des trois processus, mais jusqu’à présent, la solubilité et la stratification semblent avoir entraîné des réductions d’oxygène plus importantes que l’augmentation de la respiration aerobie. Cela devrait changer avec l’augmentation des températures mondiales, car l’impact de la chaleur sur les taux métaboliques est exponentiel. Selon une étude récente, «pour un réchauffement de 2°C, il y aura une augmentation de 29% du taux de consommation d’oxygène des océans, et pour un réchauffement de 3°C, une augmentation de 50%, ce qui entraînera une hypoxie [inadéquation entre les besoins en oxygène et les apports] des océans à grande échelle» [8].
Conséquences
«L’oxygène est fondamental pour la vie dans les océans. Le déclin de l’oxygène dans les océans est l’un des effets les plus graves des activités humaines sur l’environnement de la Terre» – Denise Breitburg, Senior Scientist, Smithsonian Environmental Research Center [9].
Un événement anoxique océanique (OAE-Oceanic Anoxic Event) est une période pendant laquelle le niveau d’oxygène dissous dans une grande partie de l’océan plonge vers (ou près de) zéro. Cela s’est produit à de nombreuses reprises au cours de la longue histoire de la Terre, la dernière fois il y a environ 94 millions d’années, lorsque la perte d’oxygène a anéanti une grande partie de la vie marine. Comme le soulignent les scientifiques associés à la Woods Hole Oceanographic Institution, les conditions océaniques actuelles sont similaires à celles qui prévalaient avant cette crise, et elles se dégradent rapidement.
«Une perturbation plus étendue semble réaliste compte tenu des émissions de carbone actuellement prévues. Sans une intervention humaine positive, les anciennes études de l’OAE sont destinées à devenir inconfortablement applicables dans un avenir pas si lointain.» [10]
Nous ne sommes pas encore dans une OAE, mais si la perte d’oxygène continue à accélérer, des extinctions à grande échelle d’espèces marines sont pratiquement certaines. Même aux niveaux actuels de désoxygénation, les dégâts sont considérables.
«Le vaste ensemble de preuves provenant des écosystèmes marins tempérés et quelques études des écosystèmes marins tropicaux démontrent que le stress de l’hypoxie entraîne souvent une simplification catastrophique des écosystèmes par la perte de biodiversité, la complexité trophique et la pêche.» [11]
En fait, toute réduction de l’oxygène disponible, et pas seulement l’hypoxie, est problématique pour la plupart des organismes vivant dans les océans. Si certains animaux marins, les méduses par exemple, sont peu affectés par la réduction de l’oxygène, d’autres connaissent un déclin lorsque le niveau baisse, même légèrement [12]. En conséquence, l’équilibre des populations dans les zones où le niveau d’oxygène baisse penche rapidement en faveur des espèces tolérantes à l’hypoxie. D’autres fuient ou meurent.
En plus de menacer directement la vie et les habitats des organismes marins, l’appauvrissement en oxygène perturbe le cycle global de l’azote. Pendant des centaines de millions d’années, les zones minimales d’oxygène naturelles ont joué un rôle clé dans le cycle de l’azote, car les bactéries qui convertissent les composés réactifs de l’azote (Nr) en gaz inerte (N2) ne sont déclenchées pour le faire qu’en l’absence d’oxygène. L’expansion des ZMO signifie que des microbes de plus en plus nombreux éliminent l’azote réactif de l’océan, déséquilibrant le cycle et réduisant la disponibilité des nutriments essentiels à la vie marine.
De plus, lorsque les bactéries convertissent l’azote réactif en N2 en présence de petites quantités d’oxygène – c’est le cas dans la plupart des ZOM – elles produisent également de l’oxyde nitreux (N2O), un gaz à effet de serre environ 300 fois plus puissant que le dioxyde de carbone et qui appauvrit également la couche d’ozone. De nombreuses études ont montré que de grandes quantités de N2O s’élevaient de la surface de l’océan au-dessus des OMZ. Il s’agit là d’une réaction positive classique – le réchauffement climatique accélère la production d’oxyde nitreux, qui à son tour accélère le réchauffement de la planète.
Enfin, il est important de garder à l’esprit que l’appauvrissement de l’oxygène ne se produit pas de manière isolée – par exemple, les organismes qui consomment plus d’oxygène augmentent également l’acidification en expirant plus de dioxyde de carbone, et les poissons qui essaient d’échapper à l’eau privée d’oxygène trouvent que les autres endroits sont trop acides.
La troisième partie de cette contribution examinera le troisième élément du trio mortel, le réchauffement des océans. Comme nous l’avons vu, l’augmentation de la température de l’eau contribue à l’acidification et à la désoxygénation, mais elle joue également un rôle direct dans la destruction des écosystèmes marins. (Article publié le 20 septembre 2020 sur le site Climate & Capitalism; traduction rédaction A l’Encontre; la troisième partie sera publiée et traduite fin octobre)
_________
[1] Howard Lee, “Ocean Oxygen – Another Climate Shoe Dropping,” Skeptical Science, May 18, 2016.
[2] Ian Angus, “Dead Zones: Industrial Agriculture versus Ocean Life,” Climate & Capitalism, August 12, 2020.
[3] L’eau froide rejoint également le Global Conveyor Belt près de l’Antarctique, et le chemin de retour transporte l’eau chaude des tropiques vers le nord. Tout «début» sélectionné sur ce vaste cycle métabolique est arbitraire.
[4] Changyu Li et al., “Increasing Escape of Oxygen From Oceans Under Climate Change,” Geophysical Research Letters, June 2020.
[5] Scientific Committee on Oceanic Research, “How Oxygen Minimum Zones Form”; A. Paulmier and D. Ruiz-Pino, “Ocean Minimum Zones (OMZs) in the Modern Ocean,” Progress in Oceanography 80, no. 3-4 (2009), 113-128.
[6] L. Caesar et al., “Observed Fingerprint of a Weakening Atlantic Ocean Overturning Circulation,” Nature 556, April 12, 2018; S. Rahmstorf, “New Studies Confirm Weakening of the Gulf Stream Circulation (AMOC),” Real Climate, September 17, 2020.
[7] Anecdote historique: la formule permettant de calculer l’effet de l’augmentation de la chaleur sur la vitesse des réactions chimiques a été découverte par Svante Arrhenius, le scientifique suédois qui a été le premier à montrer, en 1896, que les émissions de CO2 provenant de la combustion de combustibles fossiles pouvaient provoquer le réchauffement de la planète.
[8] John G. Shepherd et al., “Ocean Ventilation and Deoxygenation in a Warming World: Introduction and Overview,” Philosophical Transactions of the Royal Society A, September 07, 2017, 6.
[9] Quoted in “The Ocean Is Losing Its Breath. Here’s the Global Scope,” SERC news release, January 4, 2018.
[10] Chadlin M. Ostrander, Jeremy D. Owens, and Sune G. Nielsen, “Constraining the Rate of Oceanic Deoxygenation Leading Up to a Cretaceous Oceanic Anoxic Event (OAE-2: ~94 Ma),” Science Advances, August 9, 2017.
[11] David J. Hughes et al., “Coral Reef Survival Under Accelerating Ocean Deoxygenation,” Nature Climate Change, March 2020.
[12] Guy Claireaux and Denis Chabot, “The Significance of Ocean Deoxygenation for the Physiology of Marine Organisms,” in Ocean Deoxygenation: Everyone’s Problem, ed. D. Laffoley and J. M. Baxter (Gland, Switzerland: IUCN, 2019), 461.

Soyez le premier à commenter